THỂ TÍCH (đktc) của:
a) 0,35mol NH3
b) 0,5mol NO
c) 0,1mol NO2
THỂ TÍCH (đktc) của:
a) 0,35mol NH3
b) 0,5mol NO
c) 0,1mol NO2
\(a)V_{NH_3,đktc}=0,35.22,4=7,84l\\ b)V_{NO,đktc}=0,5.22,4=11,2l\\ c)V_{NO_2,đktc}=0,1.22,4=2,24l\)
Tìm thể tích của dung dịch HCl 2M để trong đó có hòa tan 0,5mol HCl
$V_{HCl} = \dfrac{n}{C_M} = \dfrac{0,5}{2} = 0,25(lít)$
\(V=\dfrac{n}{C_M}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
\(V_{ddHCl}=\frac{0,5}{2}=0,25(l)=250(ml)\)
Cho 20gam CaCO3 vào 200 ml dung dịch HCl 3M. Số mol khí thu được sau phản ứng là:
A. 0,6 mol.
B. 0,2 mol.
C. 0,4mol.
D. 0,5mol.
\(n_{CaCO_3}=\dfrac{20}{100}=0.2\left(mol\right)\)
\(n_{HCl}=0.2\cdot3=0.6\left(mol\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
Lập tỉ lệ :
\(\dfrac{0.2}{1}< \dfrac{0.6}{2}\) \(\Rightarrow HCldư\)
\(n_{CO_2}=n_{CaCO_3}=0.2\left(mol\right)\)
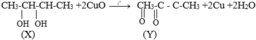
Đốt cháy hoàn toàn một lượng ancol X tạo ra 0,4mol CO2 và 0,5mol H2O. X tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam. Oxi hóa X bằng CuO tạo hợp chất hữu cơ đa chức Y. Nhận xét nào sau đây đúng với X?
A. Trong X có 3 nhóm -CH3.
B. Hidrat hóa but-2-en thu được X.
C. Trong X có 2 nhóm –OH liên kết với hai nguyên tử cacbon bậc hai.
D. X làm mất màu nước brom.
Đáp án C
Có: 0,4 mol CO2 và 0,5 mol H2O. => ancol no
nancol = 0.5 - 0.4 = 0,1 => Số nguyên tử C = 0,4/0,1 = 4 => C4H10O2
Do X tác dụng với Cu(OH)2 tạo dung dịch màu xanh lam nên X là ancol đa chức có ít nhất hai nhóm OH ở hai nguyên tử C liền kề nhau
Oxi hóa X bằng CuO tạo hợp chất hữu cơ đa chức Y => X là rượu bậc 2.
Cho 13g Zn vào một dung dịch chứa 0,5mol HCl .Tính thể tích Hidro thu được?
Ta có: \(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\\ n_{HCl}=0,5\left(mol\right)\)
PTHH: Zn + 2HCl -> ZnCl2 + H2
Theo PTHH và đề bài, ta có:
\(\frac{0,2}{1}< \frac{0,5}{2}\)
=> Zn hết, HCl dư nên tính theo nZn.
Theo PTHH và đề bài, ta có:
\(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
Thể tích H2 thu được (đktc):
\(V_{H_2\left(đktc\right)}=0,2.22,4=4,48\left(l\right)\)
PTHH
Zn + 2HCl \(\rightarrow\) ZnHCl2 +H2 \(\uparrow\)
Số mol của Zn
\(n_{Zn}\)= \(\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
Zn + 2HCl\(\rightarrow\) ZnCl2 + H2 \(\uparrow\)
1 mol 2 mol 1 mol 1 mol
0,2 mol 0,5 mol(dư) 0,2 mol
Số mol của HCl dư và dư 0,1 mol
Số mol của \(H_2\)
\(n_{H_2}\)=0,2 (mol)
Thể tích của H2 (đktc):
\(V_{H_2}\)= n . 22,4= 0,2 . 22,4 = 4,48 (lít )
cho 12.1gam hỗn hợp với 2 kim loại Zn và Fe có số mol bằng nhau vào dung dịch chứa 0,5mol HCl các phản ứng hoá học xảy ra theo sơ đồ : Zn+HCL-> ZnCl2+H2 Fe+HCl-> FeCl2+H2 a) Hỏi su phản ứng chất nào còn dư? Dư bao nhiêu gam? b)Tính khối lượng mỗi muối thu được Câu 2: Hoà tan hòn toàn 5,4g hỗn hợp bột A gồm Mg , Fe trong dung dịch HCl dư, tạo thành 3,36 lít (đktc) a)Viết các PTHH xảy ra b)Tính khối lượn muối tạo thành c)Tính khối lượng mỗi kim loại trong hỗn hợp A
Cho 5,6g Fe tac dụng hêt vơi 200ml dung dịch HCL 0,5mol
a)Viêt PTHH xảy ra
b)Tính nFe , nHCL
c) Tính "FeCL2" tạo ra
Giup
a) PTHH: Fe + 2HCl -> FeCl2 + H2
b) nHCl = 0,5.(200/1000)= 0,1(mol)
nFe= 5,6/56= 0,1(mol)
So sánh tỉ lệ: HCl hết, Fe dư tính theo nHCl.
c) => nFeCl2= nHCl= 0,1/2= 0,05(mol)
=> mFeCl2= 0,05.127= 6,35(g)
hãy tính V ở đkt của
a, hh khí gồm 6,4g khí o2 và 22,4g khí n2
b, hh khí gồm 0,75mol co2 và 0,5mol co vf 0,25mol n2
cho công thức hóa trị của muối natri hidrocacbonat NaHCO3
a, khối lượng mỗi nguyên tố có trong 0,5mol hợp chất
b,tính số nguyên tử của mỗi nguyên tố có trong 0,5mol hợp chất
`NaHCO3 ta có Na hóa trị I , HCO3 hóa trị I
a) `m NaHCO3=0,5.84=42g`
b)`mH=mC=mNa=0,5.6,02.1023=3,01.1023pt`
`mO=1,5.6,02.1023=9,045.1023pt`
a. Tính số mol của : 14g Fe, 20g Ca, 25g CaCO3, 4g NaOH, 1,5.1023phân tử H2O
b. Tính khối lượng của: 0,25mol ZnSO4, 0,2 mol AlCl3, 0,3 mol Cu; 0,35mol Fe2(SO4)3.
c. Tính thể tích của các chất khí ở đktc: 0,2mol CO2; 0,15mol Cl2; 0,3mol SO2; 0,5mol CH4.
a)
\(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
\(n_{Ca}=\dfrac{20}{40}=0,5\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)\)
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
b)
\(m_{ZnSO_4}=0,25.161=40,25\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
\(m_{Cu}=0,3.64=19,2\left(g\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0,35.400=140\left(g\right)\)
c)
\(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
\(V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
\(V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
\(V_{CH_4}=0,5.22,4=11,2\left(l\right)\)
a: \(n_{Fe}=\dfrac{14}{56}=0.25\left(mol\right)\)
\(n_{Ca}=\dfrac{20}{40}=0.5\left(mol\right)\)